Article de synthèse à destination des patients
1. Qu’est-ce qu’une rétention aiguë d’urine ?
La rétention aiguë d’urine (RAU) est une urgence urologique fréquente, surtout chez l’homme de plus de 60–70 ans.
On parle de RAU lorsqu’un homme :
- ne parvient brutalement plus à uriner,
- alors que sa vessie est pleine (globe vésical douloureux, envie intense d’uriner),
- avec souvent des douleurs importantes dans le bas-ventre, une gêne majeure, parfois des sueurs, agitation, voire des nausées.
Dans la majorité des cas chez l’homme, cette situation est liée à une hypertrophie bénigne de la prostate (HBP) qui bloque la sortie de la vessie. Mais d’autres causes sont possibles (médicaments, chirurgie récente, infection, calcul, troubles neurologiques, etc.).
Les données de la littérature rappelées par le Comité des troubles mictionnels de l’homme (CTMH) de l’Association Française d’Urologie (article 2025, Progrès en Urologie – FMC) indiquent qu’environ 1 homme sur 10 de plus de 70 ans connaîtra au moins un épisode de RAU au cours de sa vie, avec une fréquence qui augmente avec l’âge.
2. Pourquoi la RAU est-elle une urgence ?
Une vessie qui ne peut plus se vider est :
- douloureuse : tension importante de la paroi vésicale, douleurs pelviennes, parfois lombaires,
- dangereuse pour le rein : le blocage prolongé peut remonter jusqu’aux reins (reflux d’urines, altération de la fonction rénale),
- source de complications : infection urinaire, hématurie (sang dans les urines), décompensation d’un terrain fragile (cardiaque, rénal, âgé, etc.).
L’objectif immédiat est donc double :
- Soulager rapidement la douleur en vidant la vessie.
- Protéger la fonction rénale et éviter les complications.

3. Comment se passe la prise en charge initiale ?
3.1. Le diagnostic aux urgences
À l’arrivée aux urgences, le médecin :
- interroge sur les symptômes : début brutal, douleur, impossibilité totale d’uriner, antécédents d’HBP, de chirurgie, de médicaments (antidépresseurs, anticholinergiques, opioïdes, etc.),
- examine l’abdomen : il palpe souvent un globe vésical, masse tendue au-dessus du pubis,
- peut compléter par une échographie vésicale (scanner portatif de vessie) pour mesurer le volume d’urine bloqué,
- prescrit un bilan sanguin (reins, électrolytes) et parfois un examen d’urine (recherche d’infection).
Le diagnostic de RAU est clinique : impossibilité d’uriner malgré un besoin évident, vessie pleine à l’examen ou à l’échographie.
3.2. Le geste d’urgence : vider la vessie
Le traitement d’urgence est le drainage vésical, c’est-à-dire la mise en place d’un dispositif permettant aux urines de s’évacuer. Il existe deux grands modes :
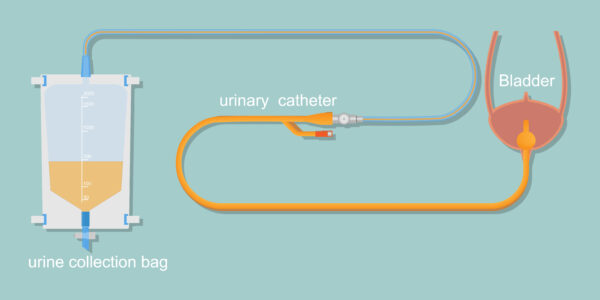
- La sonde vésicale urétrale (SV)
- Introduction d’un petit tube souple par le méat urinaire (au bout du pénis) jusque dans la vessie.
- Geste très courant, rapide, réalisé sous conditions d’asepsie.
- La sonde est maintenue en place quelques jours, reliée à une poche de recueil.
- Le cathéter sus-pubien (CSP)
- Petit tube introduit directement dans la vessie à travers la peau au-dessus du pubis, sous anesthésie locale.
- On traverse la paroi abdominale pour atteindre la vessie.
- La sonde est fixée à la peau, raccordée à une poche.
Selon la revue du CTMH (2025), ces deux modalités de drainage sont efficaces pour soulager la RAU. Le choix dépend de plusieurs paramètres.
4. Sonde urétrale ou cathéter sus-pubien : que disent les données récentes ?
4.1. Efficacité globale
Les études analysées par le CTMH ne montrent pas de supériorité claire d’une méthode sur l’autre pour la reprise des mictions à distance. En revanche, des différences existent sur le confort et certaines complications.
4.2. Avantages potentiels du cathéter sus-pubien
Les données de la littérature, rassemblées dans les recommandations 2025, suggèrent que le CSP pourrait offrir :
- un meilleur confort (absence de sonde dans l’urètre et la verge),
- moins de bactériurie asymptomatique (présence de bactéries dans l’urine sans symptômes),
- un risque d’infection urinaire possiblement plus faible que la sonde urétrale,
- la possibilité de réaliser facilement des tests de clampage (on bouche temporairement la sonde sus-pubienne pour voir si la vessie arrive à se vider par les voies naturelles).
De plus, de grandes bases de données récentes montrent que le risque de perforation intestinale lors de la pose d’un CSP, lorsqu’il est réalisé dans de bonnes conditions, est très faible (nettement inférieur à 1 %, probablement < 0,25 %).
4.3. Contre-indications et précautions
Le CSP n’est pas adapté à tous les patients. Il est contre-indiqué notamment en cas de :
- suspicion de tumeur de vessie (hématurie macroscopique inexpliquée),
- doute sur l’existence réelle d’un globe vésical (vessie pas franchement remplie),
- hématurie importante (sang rouge abondant dans les urines).
Des contre-indications relatives existent également :
- antécédent de chirurgie abdominale basse (risque d’adhérences, d’intestin collé à la vessie),
- troubles importants de la coagulation.
En revanche, le CSP est souvent préférable à la sonde urétrale en cas de :
- sténose urétrale (rétrécissement de l’urètre),
- traumatisme urétral (après chute à califourchon, par exemple),
- prostatite aiguë (infection de la prostate) où la sonde urétrale peut être très douloureuse voire contre-indiquée.
4.4. En pratique
Les recommandations 2025 ne tranchent pas en faveur d’une technique unique, mais insistent sur :
- une décision individualisée,
- la prise en compte :
- du contexte clinique,
- des contre-indications,
- des préférences du patient,
- de l’expérience du médecin.
5. Complications précoces après le drainage : ce qu’il faut savoir
Une fois la vessie drainée, certaines complications peuvent survenir :
- Hématurie (sang dans les urines)
- Fréquente après une forte distension vésicale.
- Souvent modérée, transitoire, sans gravité.
- Les études récentes montrent qu’il n’y a pas plus d’hématurie si l’on vide la vessie rapidement plutôt que progressivement.
- Syndrome de levée d’obstacle (SLO)
- Après un obstacle prolongé, les reins peuvent « se réveiller » avec une diurèse très abondante (parfois > 3 litres en 24 h).
- Risque de déshydratation et de déséquilibre en sels minéraux (sodium, potassium).
- Facteurs favorisants : très grande quantité d’urine retenue, fonction rénale déjà altérée.
- D’où la nécessité de :
- mesurer le volume initial drainé,
- surveiller la diurèse (quantité d’urine) dans les heures qui suivent,
- adapter la réhydratation (perfusion, surveillance clinique et biologique) en cas de diurèse massive.
- Chute de tension / malaise
- Rare, mais possible lors d’une levée brusque d’un obstacle très ancien.
- D’où une surveillance rapprochée, surtout chez les patients fragiles.
Les recommandations récentes valident la vidange rapide comme aussi sûre que la vidange progressive vis-à-vis de l’hématurie, mais mettent l’accent sur la surveillance de la diurèse et de l’état général dans les premières heures.
6. Alternatives à la sonde à demeure : auto-sondage et stents
6.1. Auto-sondages propres intermittents (ASPI)
Les auto-sondages propres intermittents consistent à apprendre au patient à :
- introduire lui-même une sonde urinaire à usage unique, plusieurs fois par jour,
- dans des conditions d’asepsie simplifiées (mains propres, technique enseignée),
- puis à retirer immédiatement la sonde après vidange de la vessie.
Dans le cadre de la RAU liée à l’HBP, les études montrent que :
- les ASPI offrent un bon confort au patient,
- améliorent souvent la qualité de vie par rapport à une sonde à demeure,
- pourraient favoriser une meilleure récupération de la vessie (capacité, pression, contractilité),
- sont associés à un risque d’infection urinaire au moins comparable, voire plus faible dans certaines séries que la sonde à demeure.
Le CTMH conclut que les auto-sondages sont une alternative intéressante à la sonde vésicale ou au CSP, quand le patient est apte à apprendre le geste et à le réaliser seul ou avec l’aide d’un proche.
6.2. Stents urétraux temporaires
Les stents urétraux sont de petits dispositifs insérés dans l’urètre prostatique pour maintenir le canal ouvert. Ils peuvent être proposés :
- chez des patients en échec de reprise mictionnelle avec sonde,
- lorsqu’une chirurgie de la prostate doit être retardée (terrain fragile, anticoagulants, autres pathologies à stabiliser).
Les données récentes montrent :
- un taux de reprise mictionnelle élevé sous stent,
- un risque infectieux parfois plus faible que chez les porteurs de sonde à demeure.
Mais le nombre d’études reste limité, et le CTMH estime qu’il n’y a pas assez de preuves pour les recommander de façon large à ce jour. Leur utilisation est donc cas par cas, dans des centres habitués à cette technique.
7. La rétention aiguë d’urine après une opération : qui est à risque et comment prévenir ?
Il existe une forme particulière de RAU : la rétention postopératoire, qui survient après une chirurgie (prothèse de hanche, chirurgie abdominale, hernie, chirurgie colorectale, etc.).
7.1. Facteurs de risque identifiés
Les grandes études et méta-analyses recensées par le CTMH ont mis en évidence plusieurs facteurs de risque :
- Âge > 60 ans
- Antécédent d’HBP (même modérée)
- Antécédent de RAU avant l’opération
- Type d’anesthésie :
- rachianesthésie (péridurale / spinale) plus à risque que l’anesthésie générale pour certaines chirurgies
- Utilisation importante d’opiacés (morphine, dérivés) en postopératoire
- Remplissage peropératoire trop important (beaucoup de perfusions)
- Chirurgies à risque élevé : chirurgie de hanche, genou, rectum, chirurgie pelvienne lourde
- Score ASA (score de risque anesthésique) élevé (terrain fragile)
En cas de facteurs de risque cumulés, la vigilancia après l’intervention doit être renforcée : évaluation systématique de la vessie, surveillance des mictions, recours précoce à la sonde si besoin.
7.2. Rôle préventif des alphabloquants (tamsulosine)
La tamsulosine, alphabloquant très utilisé pour les symptômes d’HBP, a été étudiée comme traitement préventif en périopératoire. Les méta-analyses récentes montrent :
- une diminution significative du risque de RAU postopératoire chez les hommes à risque recevant de la tamsulosine autour de la date opératoire.
Une étude isolée n’a pas retrouvé de bénéfice, mais deux grandes méta-analyses plaident en faveur d’un effet protecteur.
Les recommandations 2025 du CTMH indiquent que l’utilisation périopératoire de tamsulosine peut être discutée :
- chez les hommes ayant des facteurs de risque de RAU postopératoire,
- en tenant compte de la balance bénéfices / risques (effets secondaires, hypotension orthostatique possible, interactions médicamenteuses),
- idéalement en coordination entre l’urologue, l’anesthésiste et le chirurgien.
8.Le test de sevrage de la sonde : comment se fait-il en 2025 ?
Une fois la RAU soulagée par la sonde, la suite de la prise en charge vise à :
- permettre, si possible, une reprise des mictions naturelles sans sonde,
- traiter le terrain sous-jacent (HBP, médicaments, facteurs favorisants).
Le test de sevrage consiste à retirer la sonde (urétrale ou sus-pubienne) et à voir si le patient parvient à uriner spontanément avec un résidu acceptable.
8.1. Rôle fondamental des alphabloquants
Les alphabloquants (qui relâchent les muscles de la prostate et du col de la vessie) sont aujourd’hui au cœur de cette stratégie. Les molécules les plus utilisées et étudiées :
- Alfuzosine 10 mg une fois par jour
- Tamsulosine 0,4 mg une fois par jour
- Silodosine 8 mg une fois par jour
Les grandes méta-analyses montrent que, par rapport au placebo ou à l’absence de traitement, un traitement par alphabloquant avant le test de sevrage :
- augmente significativement les chances de réussite (moins de re-sondage),
- double environ la probabilité de succès dans certaines grandes séries.
Aucun alphabloquant n’a démontré de supériorité nette sur les autres : le choix dépend donc de l’expérience du médecin, du profil du patient et des effets secondaires éventuels.
8.2. Combien de temps faut-il prendre les alphabloquants avant le test ?
Les études analysées par le CTMH montrent que :
- une durée de 2 à 3 jours de traitement avant le test est déjà efficace,
- prolonger le traitement à 7 jours n’apporte pas de bénéfice clairement démontré en termes de succès du sevrage,
- un minimum de 48 heures de traitement est recommandé avant de tenter de retirer la sonde.
En pratique, on propose donc le plus souvent :
- sonde en place,
- traitement par alphabloquant pendant 2 à 3 jours,
- puis test de sevrage.
8.3. Combien de temps garder la sonde ?
Les études de cohorte montrent que :
- une durée de sondage courte (< 3–5 jours) :
- n’augmente pas le risque d’échec de reprise mictionnelle,
- est associée à moins de complications liées à la sonde (infections, fuites, obstruction, hématurie, douleurs).
Les recommandations vont donc vers :
- un test de sevrage précoce,
- généralement entre le 2ᵉ et le 5ᵉ jour suivant la mise en place de la sonde,
- plutôt que de laisser la sonde plusieurs semaines sans tenter de reprise mictionnelle.
8.4. Comment se déroule concrètement le test ?
Plusieurs modalités existent. Elles peuvent inclure :
- simple retrait de la sonde et observation,
- ou remplissage vésical préalable (par exemple avec du sérum physiologique) avant retrait, ce qui semble augmenter les chances de succès selon les méta-analyses récentes,
- mesure du volume uriné puis du résidu post-mictionnel par échographie.
Le clampage de la sonde quelques heures avant retrait, autrefois très pratiqué, n’a pas montré de bénéfice net dans les études modernes.
9.Faut-il toujours opérer après une rétention aiguë d’urine ?
Pendant longtemps, beaucoup d’hommes ayant fait une RAU étaient adressés assez rapidement à la chirurgie (résection trans-urétrale de la prostate, laser, énucléation, etc.). Les données de la littérature 2025 nuancent cette attitude.
9.1. Ce que montrent les études
- Tous les urologues ne proposent pas systématiquement une chirurgie après une première RAU.
- Après un premier épisode avec test de sevrage réussi, seule une minorité de patients (environ un quart dans certaines séries) est finalement opérée, souvent à distance.
- Les patients opérés en pleine RAU, sondés au moment de l’intervention, semblent présenter :
- plus de complications postopératoires (hémorragies, infections),
- plus de risques de transfusion,
- plus de sondages prolongés après l’intervention,
- sans véritable bénéfice fonctionnel supérieur à long terme.
Ainsi, il n’existe pas de preuve solide pour recommander de façon générale une chirurgie d’emblée après un premier épisode de RAU sans tenter de sevrage.
9.2. Quand la chirurgie devient-elle indiquée ?
Les recommandations du CTMH indiquent que la chirurgie de l’HBP est souvent indiquée lorsque :
- les épisodes de RAU sont répétitifs, malgré le traitement médical,
- il existe un échec de sevrage de la sonde (impossibilité répétée de reprendre des mictions normales),
- et/ou que l’HBP provoque d’autres complications : infections à répétition, calculs vésicaux, altération de la fonction rénale, rétention chronique avec résidu très important, gêne mictionnelle sévère et invalidante malgré traitement médical.
À l’inverse :
- un premier épisode isolé de RAU avec sevrage réussi n’est pas une indication chirurgicale automatique.
- Une discussion personnalisée s’impose, en tenant compte :
- de la taille et de l’anatomie de la prostate,
- de l’état de la vessie (paroi épaissie, diverticules…),
- de la gêne quotidienne (questionnaires IPSS, qualité de vie),
- du terrain général (âge, comorbidités, anticoagulants),
- des souhaits du patient (préférer un traitement médical prolongé ou une solution plus radicale).
9.3. Quelle technique chirurgicale privilégier ?
Les études comparant différentes techniques (résection trans-urétrale classique, bipolaire, laser, thermothérapie par micro-ondes…) chez les patients en RAU ne permettent pas, à ce jour, de désigner une technique unique comme « meilleure » dans ce contexte.
Le choix dépend :
- de la taille de la prostate,
- des habitudes et de l’expertise du centre,
- des antécédents du patient.
10. Messages clés pour les patients en 2025
Pour conclure, voici les principaux points à retenir concernant la prise en charge de la rétention aiguë d’urine chez l’homme en 2025, d’après les recommandations actualisées du CTMH :
- La RAU est une urgence : impossibilité brutale d’uriner + douleur importante = consultation immédiate (urgences, SOS médecin, appel au 15/112 selon les pays).
- Le geste prioritaire est de vider la vessie :
- par sonde urétrale ou par cathéter sus-pubien,
- le choix se fait au cas par cas, en tenant compte du contexte et des contre-indications.
- Les complications immédiates sont surveillées :
- hématurie,
- syndrome de levée d’obstacle (diurèse massive),
- troubles de la tension et des électrolytes.
- Les auto-sondages intermittents peuvent être une excellente alternative à la sonde à demeure, améliorant souvent la qualité de vie et parfois la récupération vésicale, si le patient est volontaire et apte à apprendre la technique.
- Les alphabloquants (alfuzosine, tamsulosine, silodosine) sont devenus un pilier de la prise en charge :
- pris pendant 2 à 3 jours avant le test de sevrage,
- ils augmentent nettement les chances de pouvoir retirer la sonde avec succès.
- La durée de sondage doit rester courte :
- en général moins de 3–5 jours avant un premier essai de sevrage,
- au-delà, les risques de complications liées à la sonde augmentent (infection, obstruction, douleurs, fuites).
- Le test de sevrage de la sonde est essentiel :
- il permet de savoir si la vessie peut à nouveau se vider seule,
- il est réalisé après quelques jours d’alphabloquant,
- différentes méthodes existent (retrait simple, remplissage vésical avant retrait), mais il n’est pas utile de complexifier à outrance.
- Après une opération, certaines personnes ont plus de risque de RAU :
- hommes de plus de 60 ans,
- antécédents d’HBP ou de RAU,
- rachianesthésie, chirurgie de hanche, genou, rectum,
- utilisation importante d’opiacés, perfusions abondantes.
Dans ces situations, la tamsulosine périopératoire peut être discutée avec l’équipe médico-chirurgicale pour diminuer ce risque.
- Une première RAU n’impose pas forcément la chirurgie :
- si le test de sevrage est réussi et que les symptômes restent modérés sous traitement médical,
- une simple surveillance urologique régulière peut suffire.
En revanche, récidive de RAU ou échec de sevrage répétés orientent vers une désobstruction chirurgicale (RTUP, laser, énucléation, etc.).
- La prise en charge doit être individualisée :
- chaque patient a une histoire, un terrain, des attentes différentes,
- l’urologue ajustera la stratégie (type de sonde, durée, alphabloquant, auto-sondage, chirurgie ou non) en fonction :
- de l’âge,
- des comorbidités,
- de la taille et de l’anatomie de la prostate,
- de l’état de la vessie et des reins,
- des préférences du patient (par exemple souhait d’éviter une sonde prolongée, recherche d’une solution définitive, etc.).
11. Comment se préparer et quoi demander à son urologue ?
Pour un patient ayant présenté une RAU, il est utile, lors de la consultation d’urologie, de discuter clairement des points suivants :
- Cause probable de la RAU :
- hypertrophie bénigne de la prostate seule ou facteurs associés (médicaments, chirurgie récente, infection, trouble neurologique) ?
- Stratégie pour éviter la récidive :
- traitement médical de fond (alphabloquant, ± autres médicaments de l’HBP),
- adaptation éventuelle de certains médicaments favorisants,
- surveillance régulière (clinique, PSA, échographie, débitmètre…).
- Choix du mode de drainage si une nouvelle RAU survenait :
- sonde urétrale, cathéter sus-pubien, auto-sondages,
- ce qui est le plus adapté au terrain du patient.
- Indications éventuelles de la chirurgie :
- bénéfices attendus (réduction des symptômes, prévention des récidives de RAU),
- risques (saignement, incontinence, troubles de l’éjaculation),
- délais envisageables,
- technique la plus adaptée (RTUP, laser, énucléation, autre).
Préparer, par écrit, une liste de questions ou de priorités (par exemple : « je veux éviter à tout prix de revivre une RAU », ou « je redoute surtout la chirurgie ») permet souvent d’orienter la discussion et de parvenir à une décision partagée.
12. En résumé pratique pour vos lecteurs
En 2026, la prise en charge de la rétention aiguë d’urine liée à l’HBP chez l’homme repose sur :
- un drainage vésical rapide (sonde urétrale ou cathéter sus-pubien),
- une surveillance précoce des complications de la levée d’obstacle,
- l’utilisation systématique ou quasi systématique d’un alphabloquant pendant 2–3 jours avant toute tentative de retrait de sonde,
- un test de sevrage précoce (souvent entre J2 et J5) plutôt que le maintien prolongé d’une sonde,
- une réflexion au cas par cas sur la chirurgie, proposée surtout en cas de récidives ou d’échec répété de sevrage.
Pour les patients, l’enjeu est double :
- Ne pas banaliser la rétention aiguë d’urine, qui reste une urgence.
- Comprendre que les options thérapeutiques se sont enrichies (alphabloquants, auto-sondages, meilleure évaluation du risque opératoire), permettant une prise en charge plus fine, plus personnalisée, et souvent moins invasive qu’autrefois.
En tant que chirurgien urologue, expliquer ces éléments de manière simple, en s’appuyant sur les recommandations 2026 du CTMH, permet d’impliquer le patient dans les choix de prise en charge et de réduire l’anxiété liée à cet épisode souvent très marquant qu’est une rétention aiguë d’urine.